Jerónimo Barrera Ortega.
Jefe de Sección Radiología Urológica del Hospital Clínico San Carlos de Madrid y Radiólogo Hospital Nuestra Señora del Rosario de Madrid. Urorradiología.
1. Introducción
El primer estudio de Resonancia de próstata fue en 1982, sin embargo, hasta el desarrollo de las secuencias dinámico con contrate y difusión no ha tenido una utilización determinante en el diagnóstico del Cáncer de próstata.
La estandarización de su uso viene de la mano de la implantación de una guía consensuada por un comité de expertos de la European Society of Urogenital Radiology (ESUR) y de la American College of Radiology (ACR). The Prostate Imaging Reporting and Data System (PI-RADS v2.1) es la versión actual. Esta guía estandariza la técnica de adquisición de imágenes con recomendaciones sobre los requerimientos mínimos de secuencias e interpretación de los hallazgos.
La RMmp (Resonancia Magnética multiparamétrica de próstata) es la técnica más precisa para la detección y estadificación local del carcinoma. Permite la detección y estratificación del riesgo del carcinoma clínicamente significativo.
En un porcentaje alto de los pacientes con sospecha clínica se consigue precisar la localización donde es más probable encontrar el carcinoma de cara a una biopsia más dirigida. Se utiliza en la estadificación local muy precisa de los carcinomas ya conocidos y para valorar la mejor estrategia terapéutica. También es muy útil como herramienta en el manejo de la vigilancia activa y en la recurrencia tras tratamiento.
2. Papel de la RMmp (resonancia magnética multiparamétrica) de próstata:
- Diagnóstico
- Detectar enfermedad clínicamente significativa
- Detectar carcinomas agresivos
- Especial utilidad tras una biopsia negativa y que continúa elevándose el PSA
- Minimizar el sobrediagnóstico de carcinomas indolentes
- Disminuir biopsias innecesarias debido alto valor predictivo negativo (90%)
- Tratamiento
- Estadificación local precisa
- Mejorar el diagnóstico de enfermedad que requiera tratamiento activo
- Herramienta en la Vigilancia activa
- Diagnóstico de la recurrencia tras el tratamiento
- Tras radioterapia y prostatectomía radical
3. Diagnóstico del carcinoma clínicamente significativo: PI RADS v2.1
Tiene como principal objetivo identificar carcinomas clínicamente significativos. Clasifica las lesiones en función de la combinación de los hallazgos en secuencias morfológicas y funcionales.(1)
| PI-RADS 1 | Probabilidad muy baja de presentar un carcinoma clínicamente significativo |
| PI-RADS 2 | Probabilidad baja de presentar un carcinoma clínicamente significativo |
| PI-RADS 3 | Probabilidad intermedia de presentar un carcinoma clínicamente significativo |
| PI-RADS 4 | Probabilidad alta de presentar un carcinoma clínicamente significativo |
| PI-RADS 5 | Probabilidad muy alta de presentar un carcinoma clínicamente significativo |
Informe radiológico: Debe contener la medida y localización de la lesión mostrando cual es la lesión dominante y el PI-RADS de cada una de las lesiones en orden de importancia. Se debe precisar si existe afectación tumoral extraprostática, bandeletas neurovasculares y de las vesículas seminales. Presencia de adenopatías pélvicas y metástasis óseas pélvicas.
Mapa de las lesiones: La utilización de un modelo topográfico por sectores común para urólogos, radiólogos y patólogos permite ser más precisos para localizar las lesiones identificadas en RM, con una mejor correlación patológica. Se puede utilizar el modelo de 41 regiones, en las que 38 son para la próstata y dos para las vesículas seminales y uno para el esfínter externo. La próstata se divide en derecha e izquierda por una línea sagital vertical a través de la uretra y en anterior y posterior por otra línea coronal a través de la mitad de la glándula. La zona periférica se divide en derecha e izquierda y en anterior, medial posterior y lateral posterior tanto en la base como tercio medio y del ápex. La zona de transición se divide en derecha e izquierda y en anterior y posterior tanto en la base como en el tercio medio y en el ápex. El estroma fibromuscular se divide en derecho e izquierdo tanto en la base como tercio medio y ápex. Vesículas seminales derecha e izquierda y la uretra.
Secuencias y protocolos. El estudio de la próstata se basa tanto en secuencias morfológicas potenciadas en T1 y T2 como en secuencias funcionales potenciadas en Difusión, Dinámico con contrate. (2)
Secuencias T2: Muestran un excelente detalle anatómico y de contraste en los órganos y lesiones pelvianas. Son muy útiles para la estadificación local del carcinoma. La zona periférica en la secuencia T2 es hierintensa de forma homogénea. La zona central está alrededor de los conductos eyaculadores es heterogénea de predominio hipointenso. La zona de transición se sitúa alrededor de la uretra con una señal típica glandular. El estroma fibromuscular anterior que contiene tejido fibromuscular. Con la edad se desarrolla hiperplasia benigna prostática (HBP) en la zona de transición, pudiendo adquirir un gran volumen y comprimir a la zona central. La cápsula prostática es una fina línea marcadamente hipointensa en T2 que rodea la próstata, siendo un marcador radiológico de la afectación tumoral extraprostática. La pseudocápsula o capsula quirúrgica no es una verdadera cápsula y se corresponde en T2 como un anillo marcadamente hipointenso en la interfase ente la zona periférica y la zona de transición. Las bandas neurovasculares se sitúan están situadas en la parte posterolateral de la próstata bilateralmente, a las 5 y 7 en la posición del reloj.
 Tercio medio: Corte axial T2(A). Coronal (B). Sagital(C). Zona periférica (ZP). Zona transicional (ZT). Cápsula (flecha blanca). Equipo de 3Teslas
Tercio medio: Corte axial T2(A). Coronal (B). Sagital(C). Zona periférica (ZP). Zona transicional (ZT). Cápsula (flecha blanca). Equipo de 3Teslas
Puntuación PI-RADS para la secuencia T2 en la zona periférica
| 1 | Señal normal: hiperintensa de forma homogénea |
| 2 | Imágenes lineales o de morfología en cuña o hipointensidad intermedia difusa con márgenes no perceptibles |
| 3 | Señal heterogénea o no circunscrita, redondeada hipointensidad intermedia |
| 4 | Bien delimitado y homogéneamente hipointenso focal dentro de la glándula y menor de 1,5cm |
| 5 | Bien delimitado y homogéneamente hipointenso focal dentro de la glándula ≥1.5cm o con afectación extraprostática o comportamiento invasivo |
| 1 | Señal normal: homogéneamente de intensidad intermedia o “nódulo típico” completamente encapsulado |
| 2 | Nódulo mayormente encapsulado o nódulo homogéneo circunscrito no encapsulado “nódulo atípico” o hipointensidad intermedia homogénea entre nódulos |
| 3 | Señal heterogénea o hipointensidad intermedia no bien delimitada |
| 4 | Lenticular o no circunscrita, homogéneamente con hipointensidad moderada menor de 1,5cm |
| 5 | Lenticular o no circunscrita, homogéneamente con hipointensidad moderada ≥1.5cm o afectación extraprostática o comportamiento invasivo |
 Lesión hipointensa en T2 en la zona transicional anterior derecha, flechas blancas. Puntuación 4
Lesión hipointensa en T2 en la zona transicional anterior derecha, flechas blancas. Puntuación 4
Secuencia Difusión: Es la secuencia más importante. Se adquiere con distintos valores b de potenciación en difusión. Esta secuencia y los mapas de ADC son muy importantes para la diferenciación entre el tejido tumoral con respecto al normal y con las lesiones por prostatitis. Aportan información fisiológica sobre la movilidad de las moléculas de agua, la celularidad y la integridad de las membranas información fisiológica. El coeficiente de difusión aparente ADC mide el área de moléculas de agua que se mueven por unidad de tiempo. El ADC se calcula por cada pixel de la imagen y puede ser mostrado como un mapa paramétrico.
La mayoría de los carcinomas clínicamente significativos tienen restricción de la difusión, se visualizan hipointensos con el mapa ADC con respecto el resto de la glándula e hiperintensos en difusión. El valor del ADC tiene una correlación inversa con el Gleason tumoral de tal forma que los tumores de alto grado presentan muy bajo ADC y mayor probabilidad de extensión extraprostática. (3)
Puntuación PI-RADS para la difusión con valores b altos y mapa ADC en la zona periférica y transicional
| 1 | Sin hallazgos patológicos en ADC y difusión con alto b |
| 2 | Imágenes lineales o de morfología en cuña hipointensas en ADC y/o hiperintensas en difusión con alto b |
| 3 | Lesión focal con hipointensidad intermedia en ADC y/o hiperintensa con altos valores de b |
| 4 | Lesión focal con hipointensidad marcada en ADC y marcadamente hiperintensa con altos valores de b Menor de 1,5cm de diámetro longitudinal máximo |
| 5 | Lesión focal con hipointensidad marcada en ADC y marcadamente hiperintensa con altos valores de b. Mayor de 1,5cm de diámetro longitudinal máximo o extensión clara extraprostática o comportamiento invasivo |
 Axial T2 muestra una lesión hipointensa, flecha blanca. Axial secuencia difusión con b 2500 flecha negra. Axial mapa ADC. Puntuación 4
Axial T2 muestra una lesión hipointensa, flecha blanca. Axial secuencia difusión con b 2500 flecha negra. Axial mapa ADC. Puntuación 4
Secuencia Dinámico con contraste: Se realiza con contraste de gadolinio intravenoso en el plano axial utilizando secuencias gradiente rápido 3D. El concepto de dinámico se refiere a múltiples series de imágenes recogidas después de la inyección de contraste.
Se basa en la mayor permeabilidad de los vasos tumorales al gadolinio que muestran un marcado realce precoz con respecto al tejido adyacente, debido a la angiogénesis con aumento del número de vasos, los cuales están desorganizados y tienen una permeabilidad anormal. Las lesiones malignas realzan de forma precoz y más rápido, y lavan de forma precoz que el tejido sano.
En la clasificación PI-RADS v2.1 el dinámico tiene un papel menos importante y tiene que ser interpretado juntamente con T2 y difusión. Indicará con más probabilidad carcinoma si se corresponde con una lesión focal en T2 y en difusión. El realce difuso es más típico de la prostatitis y el precoz focal del carcinoma.
Puntuación PI-RADS para la secuencia dinámica según el patrón de realce
| positivo | Realce focal y precoz coincidente con la difusión y T2 |
| negativo | Realce difuso y no precoz sin coincidir con lesiones focales en T2 o difusión. El realce focal coincide con una lesión de características de nódulo hiperplásico benigno en T2 |
 Secuencia dinámica con gadolinio. Lesión con un intenso realce precoz en la zona periférica anterior izquierda. Corresponde con realce positivo.
Secuencia dinámica con gadolinio. Lesión con un intenso realce precoz en la zona periférica anterior izquierda. Corresponde con realce positivo.
4. Estimación del Pi-RADS:
La asignación a un estudio de un valor de PI-RADS se realiza por la combinación de los distintos hallazgos de las secuencias en función de la localización de las lesiones.
Las secuencias T2 y difusión tienen mucha más importancia que la secuencia dinámica con contraste, que juega un papel inferior y que puede únicamente cambiar mínimamente la puntuación de algunas lesiones.
El realce difuso (no focal) con alteración de señal en T2 y difusión se puede ver en prostatitis. El hecho de que una lesión no tenga el típico realce precoz no añade por si misma mucha información.
En la zona periférica la secuencia dominante es la difusión por delante del T2 y del dinámico. Únicamente si la difusión tiene una puntuación de 3 y el realce es positivo puede subir a 4 el valor del PI-RADS.
Para la zona de transición el peso más importante está en el T2, que es el que determina la puntuación final del PI-RADS y también aquí con una puntuación en el T2 de 3, si la difusión es de 5, puede pasarse a un valor de PI-RADS de 4
Pi-RADS en la zona periférica:

Pi-RADS en la zona transicional:

5. Extensión extraprostática:
La valoración de la extensión tumoral extracapsular es muy importante ya que estatificación incorrecta aumenta el riesgo de recidiva tras prostatectomía radical, de recurrencia bioquímica y de pacientes con márgenes positivos.
La resonancia permite precisar el estadio T, diferenciando los tumores situados dentro de la glándula, es decir estadios inferiores o iguales aT2, de los que afectan más allá de la glándula, estadios mayores de T3. Dependiendo de este hallazgo se puede cambiar la elección de un tratamiento quirúrgico en un paciente T3 o valorar si se puede realizar tratamiento de preservación de bandeletas neurovasculares.
La RM preoperatoria puede modificar el plan inicial quirúrgico hasta en 1/3 de los casos siendo un factor pronóstico y de aproximación quirúrgica.
En la valoración de la extensión extraprostática se valora la asimetría o invasión directa del tumor y de las bandeletas neuromusculares. Los signos radiológicos más frecuentes son el abombamiento, irregularidad o espiculación del contorno prostático. La obliteración del ángulo rectoprostático es un signo muy específico. Tiene una alta especificidad (97,5%) y baja sensibilidad (50%). La RM tiene limitaciones para la detección de extensión focal (microscópica).
 Corte axial en T2 (A) y corte axial en difusión(B). Tumor en la zona periférica posterolateral izquierda (cabezas de flecha). Tumor invadiendo la bandeleta neurovascular izquierda(flechas)
Corte axial en T2 (A) y corte axial en difusión(B). Tumor en la zona periférica posterolateral izquierda (cabezas de flecha). Tumor invadiendo la bandeleta neurovascular izquierda(flechas)
Infiltración de las vesículas seminales. El diagnóstico es crítico ya que puede excluir cirugía. La RM presenta una sensibilidad en torno al 73 % y especificidad de 95%. Los criterios radiológicos de invasión son la hipointensidad en T2, el aumento del realce con contraste y la restricción de la difusión, obliteración del ángulo vesiculoprostático o la identificación de tumor invadiendo directamente la vesícula.(4)
 Cortes axiales en secuencias T2 en equipo de 3Teslas.Tumor en la zona periférica (flechas blancas). Abombamiento e interrupción de la cápsula en relación con extensión tumoral extracapsular y obliteración del ángulo rectoprostático (cabeza de flecha) (A). Otro paciente con tumor en la base prostática con invasión de las vesículas seminales (Cabezas de flechas) que están engrosadas y son hipointensas. (B)
Cortes axiales en secuencias T2 en equipo de 3Teslas.Tumor en la zona periférica (flechas blancas). Abombamiento e interrupción de la cápsula en relación con extensión tumoral extracapsular y obliteración del ángulo rectoprostático (cabeza de flecha) (A). Otro paciente con tumor en la base prostática con invasión de las vesículas seminales (Cabezas de flechas) que están engrosadas y son hipointensas. (B)
6. Limitaciones de la RM.
Los tumores de próstata que son menos visibles en RM suelen ser menos agresivos y de mejor pronóstico. Esto en la práctica reduce en número de diagnósticos de cáncer indolente. Los tumores inferiores a 0,5 cm3 son menos visibles en RM. Los tumores multifocales son menos visibles que los solitarios. Los tumores no índices también son menos visibles. El patrón cribiforme, aunque es más agresivo, sin embargo, es menos evidente en difusión por su arquitectura celular más abierta que restringe menos la difusión de las moléculas de agua. Fármacos antiandrógenos como el Duodart pueden disminuir la visibilidad de pequeñas lesiones. (5) La RM en general infraestima el volumen de los tumores.
La RM tiene falsos negativos que según distintas series están entre un 5-20 % de carcinomas significativos, aunque suelen ser pequeños o menos agresivos(6).
Tiene falsos positivos con lesiones inflamatorias catalogadas como PI RADS 4 y tumores de bajo grado catalogados como PI RADS 4 y 5. Puede haber también fallos en la fusión entre la RM y la ecografía(7)
 Lesión hipointensa en T2 e hiperimtensa en difusión. Simula un tumor. PI RADS 4. Sin embargo, corresponde con prostatitis granulomatosa por TB que muestra hallazgos similares
Lesión hipointensa en T2 e hiperimtensa en difusión. Simula un tumor. PI RADS 4. Sin embargo, corresponde con prostatitis granulomatosa por TB que muestra hallazgos similares
7. Vigilancia Activa. Seguimiento MRmp. PRECISE.
(Prostate Cancer Radiological Estimation Of Change In Sequential Evaluation)
La RM se puede utilizar como herramienta para monitorizar la vigilancia activa. La RM puede elevar el Gleason inicial de la biopsia hasta en un 36% de los casos. Identifica un posible tumor no biopsiado. Los PI RADS 1-2 pueden utilizarse como factor predictivo de un posible descenso del Gleason de 3+4 en la biopsia. Hasta en 10% de las prostatectomías disminuye el Gleason respecto a biopsia inicial. La RM puede potencialmente seleccionar a pacientes para ser candidatos a vigilancia activa debido al elevado valor predictivo negativo para detectar carcinoma clínicamente significativo.(4) PI-RADS 1-2 indican idoneidad en la selección. La incorporación de RM aumenta la detección de la progresión a alto grado durante el periodo de la vigilancia activa. Las lesiones que son más visibles en RM son las que más aumentan de grado. Todavía no es concluyente si puede sustituir a la re-biopsia. La clasificación PRECISE estima la probabilidad de progresión en vigilancia activa.(8) La European School of Oncology publicó unas recomendaciones para el seguimiento de pacientes en vigilancia activa: (PRECISE) Prostate Cancer Radiological Estimation of Change in Sequential Evaluation. (Eur Radiol. 2019 Dec 16)
| PRECISE score | Estima la probabilidad de progresión radiológica |
| 1 | Resolución de hallazgos sospechosos de cáncer previos |
| 2 | Reducción en volumen y/o visibilidad de hallazgos sospechosos de cáncer previos |
| 3 | Estable. No nuevas lesiones focales o difusas |
| 4 | Aumento significativo del tamaño y/o visibilidad de hallazgos sospechosos de cáncer previos |
| 5 | Hallazgos definitivos de progresión radiológica |
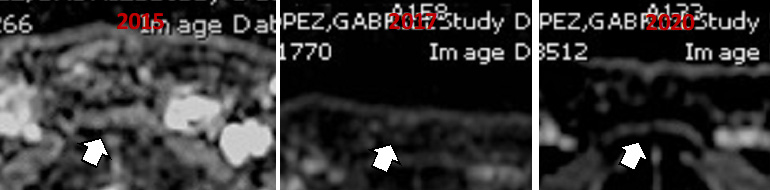 El mapa ADC muestra una lesión (flecha blanca) estable en 2015-17 (PRECISE 3) que posteriormente aumento de tamaño y con menor ADC. (PRECISE 4)
El mapa ADC muestra una lesión (flecha blanca) estable en 2015-17 (PRECISE 3) que posteriormente aumento de tamaño y con menor ADC. (PRECISE 4)
8. Recurrencia tras tratamiento (PI-RR) system
La RM tiene un importante papel para la detección y localización de la recurrencia tumoral local. La prevalencia de pacientes tratados de cáncer de próstata es alta por su alta incidencia y supervivencia. El 40% de los pacientes tratados van a desarrollar una recurrencia a lo largo de su vida por lo que el diagnóstico precoz con RM puede ayudar a elegir el mejor tratamiento.
Recientemente fruto del consenso a aparecido una guía que intenta estandarizar los criterios para evaluar la recurrencia tras tratamiento con radioterapia y prostatectomía radical. “Prostate Magnetic Resonance Imaging for Local RecurrenceReporting (PI-RR): International Consensus -based Guidelines on Multiparametric Magnetic Resonance Imaging for Prostate Cancer Recurrence after Radiation Therapy and Radical Prostatectomy”. Establece cinco categorías según la probabilidad de recurrencia. PI-RR 1 y 2 corresponden con muy baja y baja probabilidad de recurrencia. PI-RR 3 una probabilidad intermedia o incierta y PI-RR 4 y 5 con alta y muy alta probabilidad de recurrencia.(9)
Tras radioterapia la recurrencia local tiende a producirse donde primariamente estaba el carcinoma. Como consecuencia del tratamiento hay menor celularidad y vascularización con una disminución del tamaño de la próstata. En la secuencia T2 hay hipointensidad difusa de la glándula con pérdida de la anatomía zonal. En la secuencia Difusión la recidiva presenta hiperintensidad y menor ADC. La secuencia Dinámica con contrate es la más importante. El tumor realza de forma intensa y precoz.
RM tras prostatectomía radical en RM se puede identificar perianastomosis tejido fibroso y tumoral de señal diferente señal. En Difusión pueden aparecer artefactos de susceptibilidad por la cirugía. La recidiva es hiperintensa y con menor ADC. El estudio dinámico con contrate es más importante. El tumor realza de forma intensa y precoz con lavado. Es muy sensible incluso para detectar pequeños focos.
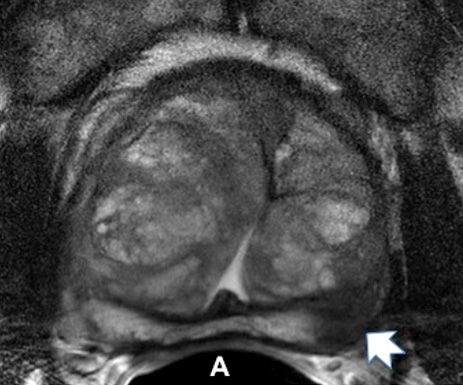
 Dos focos de recidiva tumoral local tras radioterapia (flechas blancas). Secuencia T2. Próstata heterogénea, sin diferenciación zonal, típica de los cambios post-radioterapia. Las lesiones se delimitan mal(A). Las lesiones son muy hiperintensas en la secuencia Difusión con valor de b alto(B). El mapa ADC muestra la marcada restricción de la difusión en las dos lesiones(C). Secuencia dinámica con contraste y mapa paramétrico muestra intenso realce precoz en las dos lesiones(D).
Dos focos de recidiva tumoral local tras radioterapia (flechas blancas). Secuencia T2. Próstata heterogénea, sin diferenciación zonal, típica de los cambios post-radioterapia. Las lesiones se delimitan mal(A). Las lesiones son muy hiperintensas en la secuencia Difusión con valor de b alto(B). El mapa ADC muestra la marcada restricción de la difusión en las dos lesiones(C). Secuencia dinámica con contraste y mapa paramétrico muestra intenso realce precoz en las dos lesiones(D).
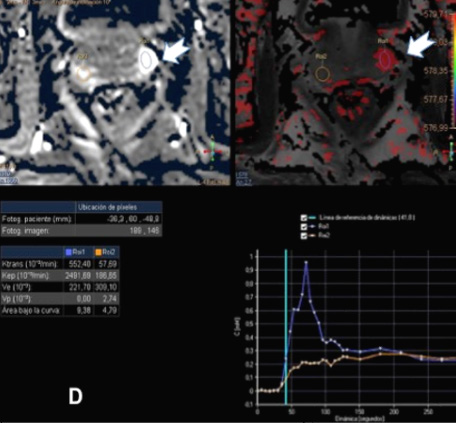
 Recidiva tumoral local en la unión vesicouretral (flecha blanca) en paciente con prostatectomía radical. La secuencia dinámica con contraste muestra un intenso realce precoz, representado en el mapa paramétrico en color rojo (A). La recidiva es muy hiperintensa en la secuencia de Difusión con valor de b alto (B). En la secuencia T2 de alta resolución en equipo de 3Teslas se identifica como una pequeña lesión de partes blanda de señal intermedia.
Recidiva tumoral local en la unión vesicouretral (flecha blanca) en paciente con prostatectomía radical. La secuencia dinámica con contraste muestra un intenso realce precoz, representado en el mapa paramétrico en color rojo (A). La recidiva es muy hiperintensa en la secuencia de Difusión con valor de b alto (B). En la secuencia T2 de alta resolución en equipo de 3Teslas se identifica como una pequeña lesión de partes blanda de señal intermedia.
9. Conclusión:
- La RMmp mejora la detección del carcinoma clínicamente significativo
- PI-RADS v2.1 establece una escala de cinco categorías en los que clasifica a las lesiones por la probabilidad de que correspondan con un carcinoma clínicamente significativo
- Es la técnica más sensible y específica para la estadificación local de los carcinomas
- Papel de la RM en la predicción pronóstica y Biomarcador de la agresividad tumoral
- Importancia de la RM en las decisiones para la selección Terapéutica
- Papel en el seguimiento en Vigilancia Activa. Clasificación PRECISE
- Papel en la recurrencia tras radioterapia y prostatectomía radical. Clasificación PI-RR
Bibliografía y enlaces de interés:
https://www.acr.org/-/media/ACR/Files/RADS/PI-RADS/PIRADS-V2-1.pdf
- Engels RRM, Israël B, Padhani AR, Barentsz JO. Multiparametric Magnetic Resonance Imaging for the Detection of Clinically Significant Prostate Cancer: What Urologists Need to Know. Part 1: Acquisition. European Urology. abril de 2020;77(4):457-68.
- Israël B, Leest M van der, Sedelaar M, Padhani AR, Zámecnik P, Barentsz JO. Multiparametric Magnetic Resonance Imaging for the Detection of Clinically Significant Prostate Cancer: What Urologists Need to Know. Part 2: Interpretation. European Urology. abril de 2020;77(4):469-80.
- Woodfield CA, Tung GA, Grand DJ, Pezzullo JA, Machan JT, Renzulli JF. Diffusion-Weighted MRI of Peripheral Zone Prostate Cancer: Comparison of Tumor Apparent Diffusion Coefficient With Gleason Score and Percentage of Tumor on Core Biopsy. American Journal of Roentgenology. abril de 2010;194(4):W316-22.
- Mehralivand S, Shih JH, Harmon S, Smith C, Bloom J, Czarniecki M, et al. A Grading System for the Assessment of Risk of Extraprostatic Extension of Prostate Cancer at Multiparametric MRI. Radiology. marzo de 2019;290(3):709-19.
- Giganti F, Moore CM, Robertson NL, McCartan N, Jameson C, Bott SRJ, et al. MRI findings in men on active surveillance for prostate cancer: does dutasteride make MRI visible lesions less conspicuous? Results from a placebo-controlled, randomised clinical trial. Eur Radiol. noviembre de 2017;27(11):4767-74.
- Mohammadian Bajgiran A, Afshari Mirak S, Shakeri S, Felker ER, Ponzini D, Ahuja P, et al. Characteristics of missed prostate cancer lesions on 3T multiparametric-MRI in 518 patients: based on PI-RADSv2 and using whole-mount histopathology reference. Abdom Radiol. marzo de 2019;44(3):1052-61.
- Lee SM, Wolfe K, Acher P, Liyanage SH. Multiparametric MRI appearances of primary granulomatous prostatitis. BJR. 9 de abril de 2019;20180075.
- Moore CM, Giganti F, Albertsen P, Allen C, Bangma C, Briganti A, et al. Reporting Magnetic Resonance Imaging in Men on Active Surveillance for Prostate Cancer: The PRECISE Recommendations—A Report of a European School of Oncology Task Force. European Urology. abril de 2017;71(4):648-55.
- Panebianco V, Villeirs G, Weinreb JC, Turkbey BI, Margolis DJ, Richenberg J, et al. Prostate Magnetic Resonance Imaging for Local Recurrence Reporting (PI-RR): International Consensus -based Guidelines on Multiparametric Magnetic Resonance Imaging for Prostate Cancer Recurrence after Radiation Therapy and Radical Prostatectomy. European Urology Oncology. diciembre de 2021;4(6):868-76.